我们的产品组合及管线涵盖已上市药物、后期临床候选药物及处于创新前沿的早期发现项目。
我们拥有四款已上市药物:泽普生®(甲苯磺酸多纳非尼片),为中国首款本土研发用于晚期肝癌一线治疗的小分子多靶点药物;泽普平®(盐酸吉卡昔替尼片),为中国首款本土研发用于治疗骨髓纤维化的创新型JAK抑制剂;泽普凝®(重组人凝血酶),为中国唯一采用重组DNA技术研发并成功商业化的重组人凝血酶;以及泽速宁®(注射用人促甲状腺素beta)为中国首个获批用于分化型甲状腺癌术后精准评估的创新产品。
•泽普生®(甲苯磺酸多纳非尼片): 于2021年6月在中国获批的首款用于晚期HCC一线治疗的国产小分子多靶点药物,其获批依据为III期临床试验中展现的生存获益改善。此外,泽普生®是晚期肝癌头对头临床试验中唯一展现出优于索拉非尼生存获益的单药疗法。于2022年8月,泽普生®进一步获批用于进展性、局部晚期或转移性放射性碘难治性分化型甲状腺癌治疗。两项适应症均已纳入国家医保药品目录。凭借疗效提升及整体安全性良好的特点,该药物已被近30部肝癌、甲状腺癌相关国家级诊疗指南及专家共识推荐作为一线治疗方案。
•泽普平®(盐酸吉卡昔替尼片):于2025年5月获批骨髓纤维化适应症,泽普平®具有独特作用机制,同时靶向JAK及激活素A受体1型(“ACVR1”),显著提升疗效与安全性;已被《2025年中国临床肿瘤学会(“CSCO”)恶性血液病诊疗指南》推荐作为骨髓纤维化一线治疗方案,并被推荐为合并贫血患者的优选治疗药物。2026年1月,泽普平®纳入国家医保药品目录。泽普平®同时在多个具有巨大市场潜力的自身免疫性适应症中积极推进临床开发,基于III期临床试验的积极结果,其重度斑秃适应症目前正在接受NDA审评,使其成为该领域研发进度最领先的国产JAK抑制剂之一。此外,强直性脊柱炎III期临床试验近期已达到主要终点,中重度特应性皮炎III期临床试验正在进行中,两项适应症均蕴藏重大市场机会。
•泽普凝®(重组人凝血酶):于2024年1月获批上市,并于2025年1月纳入国家医保药品目录。已被中国医师协会骨科医师分会关节外科学组2025年《髋膝关节置换术止血专家共识》推荐。
• 泽速宁®(注射用人促甲状腺素beta):于2026年1月获批上市,用于分化型甲状腺癌患者在甲状腺全切或近全切除术后随访中的协同诊断,以进行血清甲状腺球蛋白(Tg)检测,伴或不伴放射性碘(131I) 全身显像(WBS)检查,填补了国内分化型甲状腺癌术后精准评估的市场空白。
截至2025年12月,我们策略层级分明的候选药物管线包含近30项主要临床项目的10余款候选药物(包括泽普平®及其自身免疫性疾病相关临床项目)。其中,已有3款候选药物的7项适应症进入BLA/NDA或关键/III期注册临床试验阶段,包括目前正在推进的泽普平®重度斑秃、强直性脊柱炎及特应性皮炎适应症的III期临床试验,这将使其适应症范围拓展至自身免疫性疾病领域。
我们持续投入新靶点及突破性技术研发,重点项目包括ZG006(Alveltamig)(全球首款靶向DLL3的三特异性抗体,具有best in class潜力)及ZG005(Nilvanstomig)(PD-1/TIGIT双特异性抗体,为全球进展最领先的项目之一,同样具备best in class及first in class潜力)。特别是在肿瘤领域,我们正开发创新联合疗法,充分发挥产品组合与研发管线的协同优势,并采取专注策略以满足全球对难治性及复发性癌症未满足的需求,包括通过联合疗法克服PD-1抗药性。我们的每项核心资产为全球业务拓展及合作机会奠定坚实价值基础。
此外,我们亦在构建前沿早期项目组合,包括ZGGS18、ZGGS34、ZGGS15、ZG2001、ZG0895、ZG016及ZG2273,覆盖T细胞衔接器、双特异性及多特异性抗体,以及针对传统“不可成药”靶点的小分子疗法。该等项目体现了我们深厚的技术实力,以及将持续的科学投入转化为突破性创新的能力。
随着管线不断扩充及后期项目持续推进,我们为未来商业增长奠定良好基础。我们始终致力于研发拥有全球知识产权、安全、有效且可及的创新药物,旨在解决中国及全球范围内重大未被满足的临床需求。
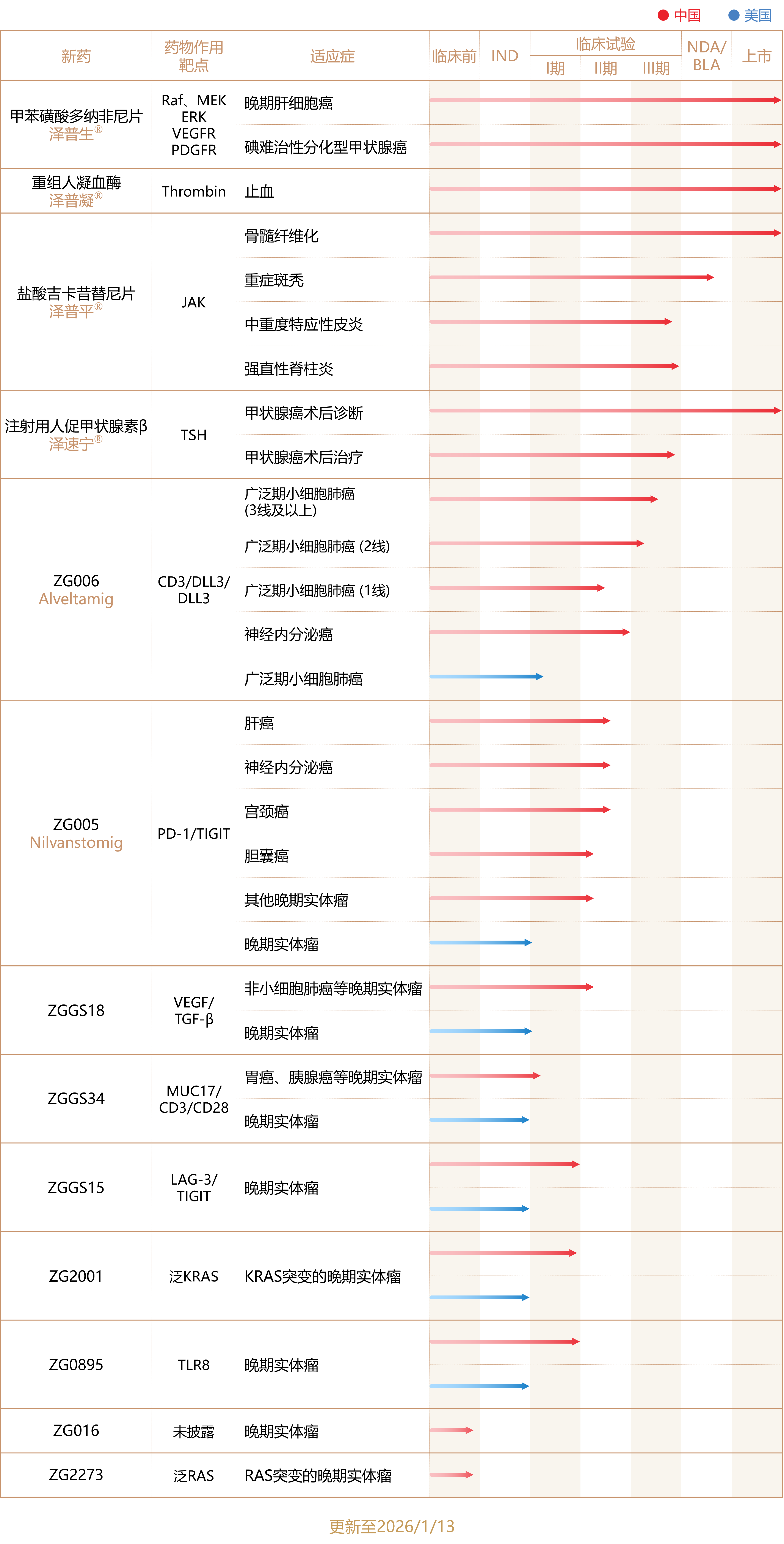
下图概述于截至2026年1月我们已上市产品及核心候选药物的研发进展: